
國重室分子影像與核醫(yī)學(xué)研究中心李楨團(tuán)隊(duì)發(fā)現(xiàn)牛血清白蛋白(BSA)修飾的Cu2?xSe納米顆粒聯(lián)合近紅外光照能顯著促進(jìn)神經(jīng)干細(xì)胞定向分化為神經(jīng)元,補(bǔ)充帕金森小鼠腦內(nèi)丟失的神經(jīng)元并恢復(fù)其功能,從而提高帕金森病的治療效果。相關(guān)成果以“Modulating efficient differentiation of neural stem cells into neurons by using plasmonic nanoparticles and the NIR II irradiation to boost therapy of Parkinson’s disease”為題發(fā)表在Nano Today雜志上。
帕金森病是目前全球第二大神經(jīng)退行性疾病,其常見的發(fā)病機(jī)制包括路易小體沉積、線粒體功能障礙、氧化應(yīng)激和神經(jīng)炎癥等等。這些發(fā)病機(jī)制會(huì)相互促進(jìn)和串?dāng)_,最終導(dǎo)致中腦黑質(zhì)致密部區(qū)域多巴胺能神經(jīng)元的進(jìn)行性損傷和丟失,繼而引起黑質(zhì)-紋狀體系統(tǒng)功能減退、多巴胺含量降低,從而促進(jìn)帕金森病的發(fā)生與發(fā)展。因此,補(bǔ)充丟失的神經(jīng)元是治療帕金森病的重要策略之一。
神經(jīng)干細(xì)胞是源于中樞神經(jīng)系統(tǒng)的多能干細(xì)胞,具有自我更新和多向分化潛能,為治療帕金森病提供了良好機(jī)遇。神經(jīng)干細(xì)胞能夠分化成神經(jīng)元、星形膠質(zhì)細(xì)胞和少突膠質(zhì)細(xì)胞。然而,神經(jīng)干細(xì)胞在無干擾下自然分化為神經(jīng)元的效率較低,很難實(shí)現(xiàn)對(duì)神經(jīng)損傷修復(fù)、促進(jìn)神經(jīng)再生以及治愈帕金森病等目的。因此,如何調(diào)控神經(jīng)干細(xì)胞高效定向分化為神經(jīng)元是神經(jīng)干細(xì)胞治療帕金森病的關(guān)鍵科學(xué)問題之一。
在前期工作中,分子影像與核醫(yī)學(xué)研究中心李楨團(tuán)隊(duì)構(gòu)建了基于Cu2-xSe的多功能納米顆粒,用于調(diào)控小膠質(zhì)細(xì)胞和神經(jīng)元功能而提高帕金森病的治療效果。首先,研究團(tuán)隊(duì)構(gòu)建了靶向小膠質(zhì)細(xì)胞、具有多重類酶活性的CSPQ仿生納米顆粒,通過將小膠質(zhì)細(xì)胞極化為具有神經(jīng)保護(hù)作用的M2表型,緩解氧化應(yīng)激引起的帕金森癥狀(J.Am.Chem.Soc.2020,142,21730?21742)。其次,研究團(tuán)隊(duì)在Cu2-xSe納米顆粒表面耦聯(lián)TRPV1抗體,利用Cu2-xSe優(yōu)異的光熱轉(zhuǎn)化效應(yīng)可控開啟小膠質(zhì)細(xì)胞表面的TRPV1離子通道,促進(jìn)Ca2+內(nèi)流而增強(qiáng)小膠質(zhì)細(xì)胞的自噬水平和降解神經(jīng)元外α-突觸核蛋白聚集體的能力,進(jìn)而改善帕金森病小鼠的運(yùn)動(dòng)和記憶能力(Adv. Mater.2022,34,2108435)。
由于α-突觸核蛋白聚集體在神經(jīng)元內(nèi)形成,因此,阻止神經(jīng)元內(nèi)α-突觸核蛋白發(fā)生病變聚集和及時(shí)清除α-突觸核蛋白聚集體是從根本上解決α-突觸核蛋白聚集體問題的重要策略。研究團(tuán)隊(duì)發(fā)現(xiàn)CSPQ納米顆粒可以通過激活神經(jīng)元Nrf2/Keap1/p62信號(hào)通路,促進(jìn)神經(jīng)元降解α-突觸核蛋白聚集體并改善由其引起的帕金森癥狀(Nano Today 2023,49,101770)。此外,研究團(tuán)隊(duì)還構(gòu)建了靶向神經(jīng)元線粒體的超小納米顆粒,通過激活受損神經(jīng)元的SIRT1/PGC-1α信號(hào)通路,介導(dǎo)線粒體生物發(fā)生,緩解神經(jīng)元線粒體功能障礙從而改善帕金森病癥狀(Adv.Sci.2023,e2300758)。
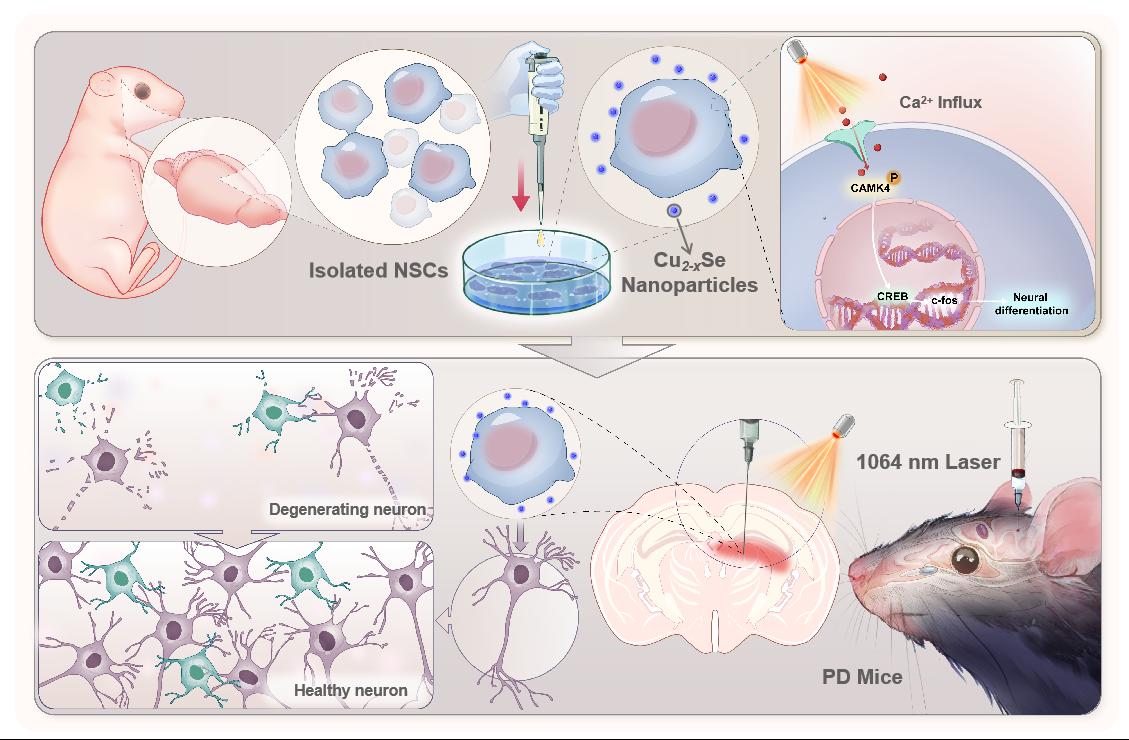
圖1. Cu2-xSe納米顆粒聯(lián)合1064 nm激光調(diào)控神經(jīng)干細(xì)胞定向分化為神經(jīng)元,治療帕金森病小鼠的示意圖。
基于上述基礎(chǔ),研究團(tuán)隊(duì)發(fā)現(xiàn)Cu2-xSe納米顆粒聯(lián)合1064 nm近紅外激光作用能夠開啟神經(jīng)干細(xì)胞膜表面的電壓門控鈣離子通道(VGCC),促進(jìn)Ca2+內(nèi)流,激活神經(jīng)干細(xì)胞,并通過Ca2+/CaMK/CREB/c-Fos通路促進(jìn)神經(jīng)發(fā)生進(jìn)程,最終達(dá)到調(diào)控神經(jīng)干細(xì)胞加速定向分化為成熟的功能性神經(jīng)元的目的(圖1)。本研究為治療帕金森病或其它神經(jīng)元功能損傷相關(guān)疾病提供了新思路。