
阿爾茨海默病是一種常見的神經退行性疾病,以進行性認知障礙為特征,對患者的生命和健康構成嚴重威脅。近期研究發現,阿爾茨海默病影響了全球5000多萬人,預計2050年將超過1.52億人。現有藥物治療效果有限,難以逆轉突觸和神經元的損失,且副作用明顯。減少淀粉樣蛋白β或tau蛋白的策略對阿爾茨海默病沒有明顯效果,不能恢復受損的神經組織。最近有研究表明,神經干細胞可自我更新、分化和遷移,增強突觸可塑性和神經發生。因此,它們被認為是一種有吸引力的阿爾茨海默病再生治療方法。
來自中國天津中醫藥大學第一附屬醫院趙嵐團隊在《中國神經再生研究(英文版)》(Neural Regeneration Research)上發表綜述。該綜述發現,神經可塑性可在整個生命期存在,且隨著年齡的增長而其能力不斷下降,且在衰老和阿爾茨海默病患者中受損明顯。因此,促進神經可塑性可能是緩解阿爾茨海默病的一個有前途的策略。神經干細胞不僅能減輕淀粉樣蛋白β和tau蛋白水平,也能促進突觸可塑性和神經發生以修復哺乳動物大腦的微環境,這被認為是改善阿爾茨海默病有巨大潛力的新療法。
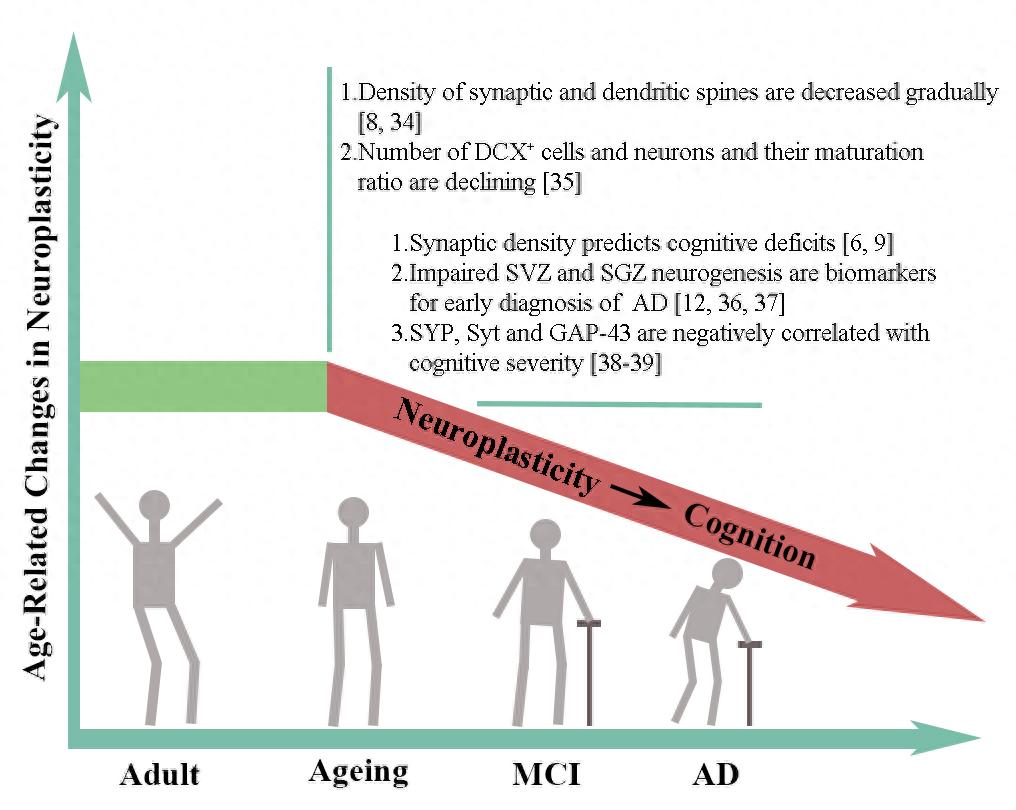
阿爾茨海默病是一種毀滅性的神經退行性疾病,現有藥物只能暫時緩解癥狀,無法治愈阿爾茨海默病,亟需要安全且有效的治療藥物。神經干細胞具有強大的更新、分化、增殖能力,其能否緩解阿爾茨海默病認知以及記憶缺陷值得深入的研究。趙嵐等通過對阿爾茨海默病臨床和臨床前樣本研究進行分析,發現阿爾茨海默病神經可塑性顯著受損,具體表現為突觸可塑性和神經發生受損。突觸可塑性受損表現為阿爾茨海默病患者和小鼠模型海馬和前額葉皮質長時程增強、突觸密度、突觸連接和樹突棘密度以及突觸后致密物95、突觸素、腦源性神經營養因子和TrkB蛋白表達均明顯降低。研究發現,早期阿爾茨海默病神經發生受損,且隨著阿爾茨海默病癥狀的加重,成年海馬神經發生急劇下降,特別是神經元丟失,這與神經前體細胞存活、增殖和分化能力降低有關,也與腦源性神經營養因子和TrkB表達減少有關。上述研究表明,阿爾茨海默病神經可塑性受損嚴重,這是其發病的關鍵原因,恢復和/或促進海馬神經可塑性可能是預防和治療阿爾茨海默病,特別是輕度認知障礙的一種有吸引力的策略。
鑒于神經干細胞可分化為神經元、星形膠質細胞和少突膠質細胞,并進行自我更新,為腦組織提供大量神經元。這決定了神經干細胞在神經退行性疾病中的治療潛力。神經干細胞有效治療疾病的關鍵階段包括遷移、存活、定向增殖和分化、逆轉丟失神經元和突觸。進一步分析發現,神經干細胞的遷移和增殖能力主要由多種因素決定,包括生長因子、細胞因子以及供體細胞的分化狀態。因此,調節生長因子和細胞因子水平以及供體細胞分化階段對神經干細胞遷移、存活和增殖能力有促進作用。但是研究發現阿爾茨海默病內源性神經干細胞數量和功能下降。內源性修復功能不足以補償中樞神經系統中受損的神經干細胞,這可能與阿爾茨海默病的經典病理淀粉樣蛋白β和(或)tau有關。因此,當務之急是探索能夠減少淀粉樣蛋白β和(或)tau表達的方法,以調節和維持阿爾茨海默病患者腦組織中內源性神經干細胞的正常平衡和再生潛力。
而后,趙嵐等對神經干細胞治療阿爾茨海默病的小鼠模型進行了簡述,發現阿爾茨海默病小鼠模型主要包括5×FAD、3×Tg、APP/PS1、Tg2576、SAMP8、CaM/Tet-DTA小鼠等。阿爾茨海默病小鼠模型為藥物研發提供了重要的依托。未來有必要在多種動物模型中進行臨床前實驗,直到有更完整的阿爾茨海默病動物模型,以確保臨床前結果能更好地轉化進臨床。此外,對阿爾茨海默病的關鍵腦區進行靶向給藥仍然是一個尚未解決的重大挑戰,鮮有研究對神經干細胞的給藥方式進行總結和分析。給藥途徑對神經干細胞的生物分布和療效有重要影響。趙嵐等發現阿爾茨海默病的主要給藥方式包括鼻內、腦室內、靜脈內和口服,這在臨床應用中各有優缺點,而神經干細胞最佳給藥方式仍有待深入的探索。
接下來,趙嵐等深入分析了神經干細胞移植對阿爾茨海默病小鼠神經可塑性的影響,結果發現,神經干細胞可逆轉阿爾茨海默病小鼠大腦皮質和海馬中的突觸損失,增加可塑性相關分子表達,但具體機制仍不清楚。有學者發現,敲除神經干細胞來源的腦源性神經營養因子可降低突觸素水平,但不能改善3xTg阿爾茨海默病小鼠認知障礙和海馬中突觸的密度。這提示神經干細胞促進突觸可塑性的機制可能與腦源性神經營養因子調節密切相關。而過表達腦源性神經營養因子的神經干細胞可增強長時程增強,并增加突觸密度,提高海馬中突觸后致密物95、突觸素和腦源性神經營養因子蛋白水平,促進更多成熟的顆粒細胞進入顆粒細胞層,促進外源性神經干細胞與內源性細胞形成新的突觸連接。綜上所述,腦源性神經營養因子在神經干細胞增強海馬突觸可塑性方面發揮了關鍵的作用。研究發現,外源性神經干細胞可在阿爾茨海默病小鼠海馬中存活,并分化成神經元和星形膠質細胞,遷移到病變部位,修復和替換丟失的神經元,并促進新神經元與功能性神經回路的整合,最終形成功能性神經元并整合到神經回路中,這與神經干細胞介導的神經營養因子促進成年海馬神經發生有關。
雖然神經干細胞通過調節神經可塑性來改善認知記憶方面顯示出了巨大的潛力,但是神經干細胞臨床轉化卻存在一些阻力。趙嵐等發現神經干細胞來源的細胞外囊泡可緩解病理特征,包括淀粉樣蛋白β和神經炎癥,并促進神經可塑性,緩解阿爾茨海默病認知缺陷,且無明顯不良反應。神經營養因子可促進神經干細胞的生存、增殖和分化能力,提高突觸和樹突棘密度及可塑性相關分子表達,抑制神經炎癥,并促進受損組織的內源性修復。膽堿乙酰轉移酶或中性內肽酶能促進海馬和皮質中神經干細胞遷移、存活和分化能力,逆轉神經遞質和神經營養因子的不足,并減少淀粉樣蛋白β和神經炎癥,進而改善學習和記憶能力。
最后,臨床前研究已證實神經干細胞治療阿爾茨海默病的安全性和有效性,但目前臨床研究依然較少。臨床前研究發現,鼻內移植人神經干細胞可減輕APP/PS1小鼠的認知障礙,且無明顯不良反應。這表明鼻內給藥人神經干細胞是一種非侵入性的阿爾茨海默病治療策略。此外,從已發表的研究結果來看,神經干細胞治療阿爾茨海默病的臨床效果是有限的。這可能與一些因素密切相關。首先,最佳給藥途徑的選擇似乎是關鍵。不同的給藥途徑,如經腦室內、鼻腔和靜脈途徑,都會影響干細胞在大腦中的存活和分化。其次,盡管神經干細胞治療阿爾茨海默病是可行的,但其安全性需要不斷驗證和完善,在轉化為臨床試驗前仍需開發安全策略。最后,神經干細胞的制備質量也需要進行更深入的研究,應從細胞制備中的酶、蛋白質和基因等多個層面進行探討。
隨著年齡的增長,神經可塑性受損越來越嚴重,這是早期預測及診斷阿爾茨海默病的一個有效標志。早期阿爾茨海默病神經可塑性已經受損,所以檢測衰老和阿爾茨海默病的神經可塑性是否受損,有利于提高阿爾茨海默病的早期診斷率。神經干細胞具有自我更新、多向分化、免疫原性低、歸巢能力強以及免疫調節和旁分泌功能等優點。神經干細胞通過旁分泌作用分泌可塑性相關分子,促進神經發生、突觸發生。重要的是,神經干細胞移植可從根本上逆轉阿爾茨海默病神經元和突觸的丟失。此外,神經干細胞還可以減輕阿爾茨海默病的典型病理變化,如淀粉樣蛋白β和tau及神經炎癥。因此,神經干細胞調節神經可塑性可能是一種有前途的阿爾茨海默病再生療法。
臨床前研究顯示神經干細胞療法是安全有效的,但許多臨床試驗卻失敗了。這表明在基礎實驗臨床轉化前,仍有許多障礙需要克服,如安全性、細胞來源和最佳治療時間和給藥途徑。盡管存在這些障礙,趙嵐等仍建議加快神經干細胞的轉化研究,這將有利于研究阿爾茨海默病的病因和潛在的治療方法。神經干細胞來源的細胞外囊泡、神經營養因子調節以及神經干細胞基因修飾可逆轉神經元和突觸的缺失,緩解阿爾茨海默病病理表現,這將為阿爾茨海默病患者提供安全的、具有臨床轉化意義的療法。相信在不遠的將來,隨著科學技術的不斷進步,神經干細胞將成為一種真正有益的臨床療法,為阿爾茨海默病患者帶來福音。