
近日,中國科學院廣州生物醫藥與健康研究院研究員潘光錦團隊在人多能干細胞來源基因工程化巨噬細胞抗腫瘤研發中取得新進展,研究提供了一種大規模生產用于實體瘤治療的基因工程化巨噬細胞策略,并開發出一種功能增強型抗腫瘤基因工程化巨噬細胞。相關成果發表于《分子治療—方法與臨床開發》。
巨噬細胞可以被募集并駐留在腫瘤微環境中,在腫瘤發生過程中發揮重要作用。與T細胞、NK細胞等其他免疫細胞相比,巨噬細胞具有更好的腫瘤浸潤能力,近年來其在實體瘤治療中引起廣泛的關注。腫瘤微環境存在多種免疫抑制機制,因此,基因工程化巨噬細胞已成為調節腫瘤微環境,治療癌癥的一種新型策略。然而,巨噬細胞來源受限和基因修飾操作難等問題限制了巨噬細胞療法廣泛應用。因此,開發更有效的方法來克服這些限制對于基因工程化巨噬細胞治療實體瘤至關重要。
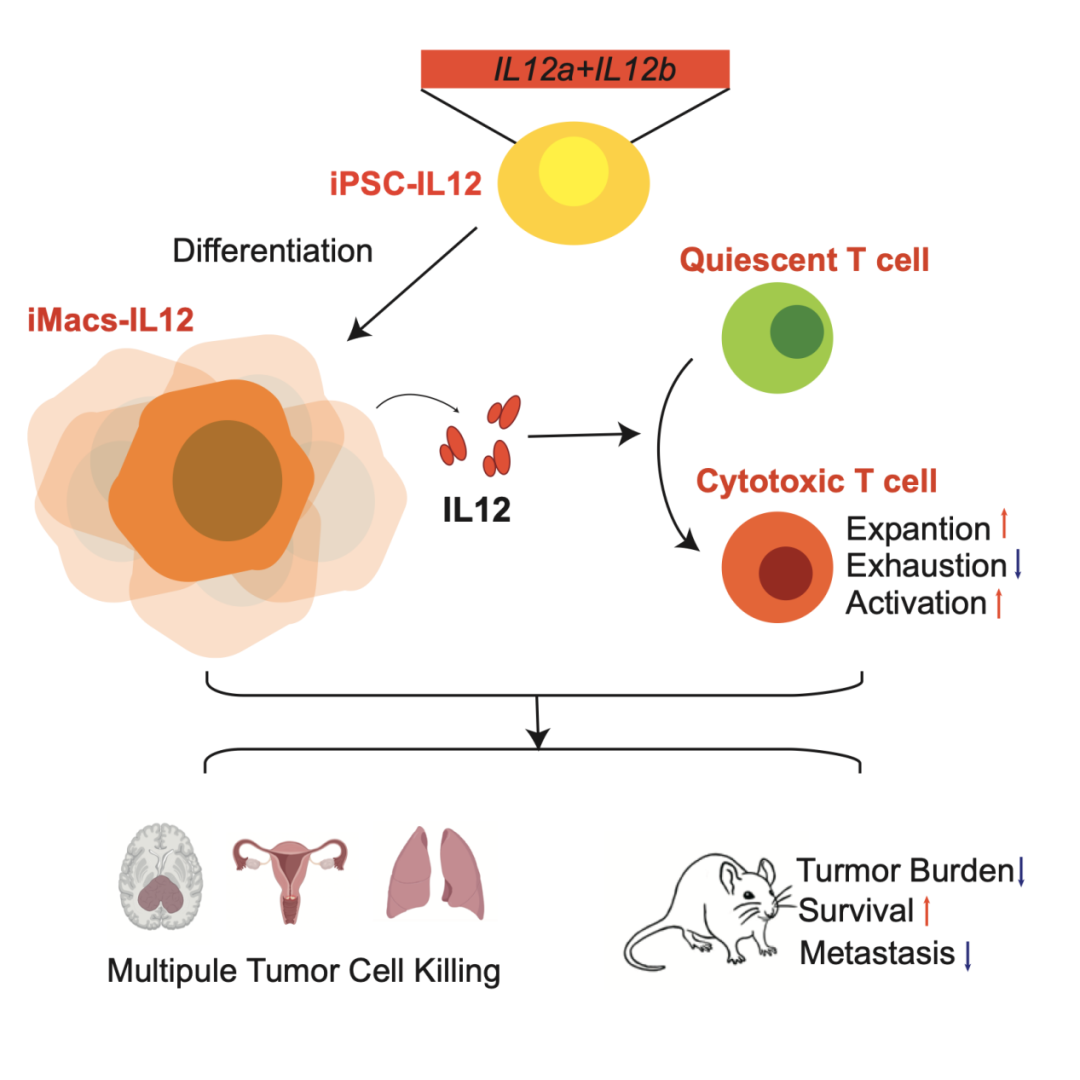
該研究利用人多能干細胞定向體外誘導分化產生成熟巨噬細胞,從1個T150培養瓶106個人多能干細胞開始,1個月內可產生109個以上的成熟巨噬細胞,從而克服細胞來源的局限性。研究者利用人多能干細胞無限自我更新的特性,通過基因編輯將IL12的基因靶向整合到人多能干細胞的特異性安全位點上,隨后通過上述分化體系產生穩定分泌IL12的基因工程化巨噬細胞(iMac_IL12)。成熟巨噬細胞及成熟巨噬細胞_IL12表達巨噬細胞相關標識物,具有典型的巨噬細胞特性,如吞噬和極化,在轉錄組水平與人外周血單核細胞來源的巨噬細胞相似。白細胞介素12(IL12)通過刺激NK細胞和T細胞來促進免疫,具有改善腫瘤微環境的極大潛力。但是IL12的半衰期短,且系統給藥副作用較大。研究者發現通過靜脈移植,成熟巨噬細胞_IL12可以在小鼠體內被招募并穩定駐留在實體瘤組織中,降低其副作用。
接下來,研究者發現成熟巨噬細胞_IL12可以誘導PBMCs產生大量IFN-γ以增強免疫。在體外及體內實驗中,成熟巨噬細胞_IL12對CD8+T細胞的維持、增殖和激活均具有積極作用,并且可以抑制T細胞的耗竭。此外,iMac_IL12顯著促進T細胞對宮頸癌、神經膠質瘤和肺癌等腫瘤細胞系的殺傷。在小鼠CDX模型中,iMac_IL12聯合T細胞可以顯著抑制小鼠的腫瘤生長并延長生存周期,并在小鼠腫瘤轉移模型中同樣可以顯著降低腫瘤負荷,延長生存周期,并減少腫瘤細胞向主要臟器轉移。
該研究分化的成熟巨噬細胞可以克服巨噬細胞產品臨床應用面臨的的來源障礙,避免了巨噬細胞在基因編輯和病毒整合中的安全性和低效性等問題。該基因工程化巨噬細胞顯示出T細胞依賴的強抗腫瘤作用,可以顯著抑制腫瘤生長和系統性轉移,提高癌癥存活率,為基因工程化巨噬細胞的研發和應用提供了新的思路。